Page 191 - Hóa phân tích
P. 191
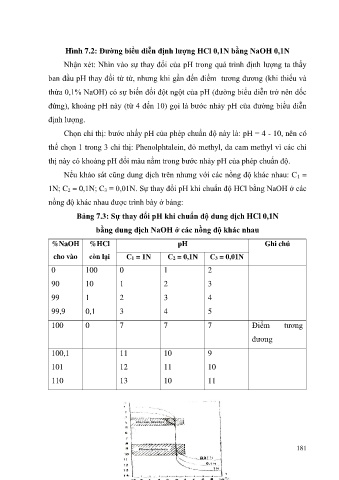
Hình 7.2: Đường biểu diễn định lượng HCl 0,1N bằng NaOH 0,1N
Nhận xét: Nhìn vào sự thay đổi của pH trong quá trình định lượng ta thấy
ban đầu pH thay đổi từ từ, nhưng khi gần đến điểm tương đương (khi thiếu và
thừa 0,1% NaOH) có sự biến đổi đột ngột của pH (đường biểu diễn trở nên dốc
đứng), khoảng pH này (từ 4 đến 10) gọi là bước nhảy pH của đường biểu diễn
định lượng.
Chọn chỉ thị: bước nhẩy pH của phép chuẩn độ này là: pH = 4 - 10, nên có
thể chọn 1 trong 3 chỉ thị: Phenolphtalein, đỏ methyl, da cam methyl vì các chỉ
thị này có khoảng pH đổi màu nằm trong bước nhảy pH của phép chuẩn độ.
Nếu khảo sát cũng dung dịch trên nhưng với các nồng độ khác nhau: C 1 =
1N; C 2 = 0,1N; C 3 = 0,01N. Sự thay đổi pH khi chuẩn độ HCl bằng NaOH ở các
nồng độ khác nhau được trình bày ở bảng:
Bảng 7.3: Sự thay đổi pH khi chuẩn độ dung dịch HCl 0,1N
bằng dung dịch NaOH ở các nồng độ khác nhau
%NaOH %HCl pH Ghi chú
cho vào còn lại C1 = 1N C2 = 0,1N C3 = 0,01N
0 100 0 1 2
90 10 1 2 3
99 1 2 3 4
99,9 0,1 3 4 5
100 0 7 7 7 Điểm tương
đương
100,1 11 10 9
101 12 11 10
110 13 10 11
181