Page 76 - Hóa phân tích
P. 76
Nhìn vào sự thay đổi của pH trong quá trình định lượng ta thấy ban đầu pH
thay đổi từ từ, nhưng khi gần đến điểm tương đương (khi thiếu và thừa 0,1%
NaOH) có sự biến đổi đột ngột của pH (đường biểu diễn trở nên dốc đứng),
khoảng pH này (từ 4 đến 10) gọi là bước nhảy pH của đường biểu diễn định lượng
(đường cong chuẩn độ). Vì vậy, có thể sử dụng các chỉ thị thông thường:
phenolphtalein (8-10); methyl đỏ (4,2-6,4), bromotimol xanh và methyl da cam
(3,1-4,4) để nhận ra điểm tương đương (các chỉ thị này có khoảng pH đổi màu nằm
trong bước nhảy pH của đường cong chuẩn độ).
* Ảnh hưởng nồng độ NaOH trong phép chuẩn độ:
Nếu khảo sát dung dịch HCl trên nhưng với các nồng độ khác nhau: C 1 =
1N; C 2 = 0,1N; C 3 = 0,01N. Sự thay đổi pH khi chuẩn độ HCl bằng NaOH ở các
nồng độ khác nhau được trình bày ở hình 7.2.
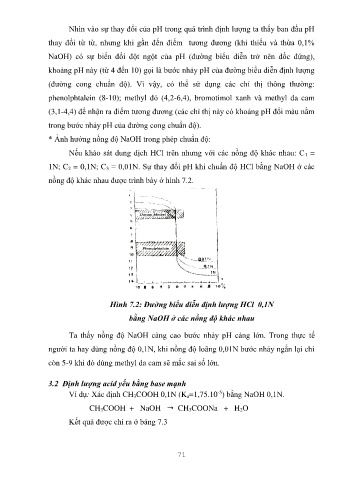
Hình 7.2: Đường biểu diễn định lượng HCl 0,1N
bằng NaOH ở các nồng độ khác nhau
Ta thấy nồng độ NaOH càng cao bước nhảy pH càng lớn. Trong thực tế
người ta hay dùng nồng độ 0,1N, khi nồng độ loãng 0,01N bước nhảy ngắn lại chỉ
còn 5-9 khi đó dùng methyl da cam sẽ mắc sai số lớn.
3.2 Định lượng acid yếu bằng base mạnh
-5
Ví dụ: Xác định CH 3COOH 0,1N (K a=1,75.10 ) bằng NaOH 0,1N.
CH 3COOH + NaOH CH 3COONa + H 2O
Kết quả được chỉ ra ở bảng 7.3
71